Compoziția chimică a celulelor
Conţinut

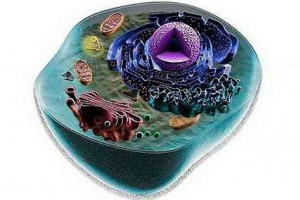
Celulă - unitate elementară de viață pe pământ. Are toate semnele unui organism viu: crește, multiplică, schimburi cu substanțele și energia de mediu, reacționează la stimulii externi. Începutul evoluției biologice este asociat cu apariția formelor celulare de viață pe pământ. Organismele unicelulare sunt celulele existente separat unul de celălalt. Corpul tuturor animalelor și plantelor multicelulare - construite din mai multe sau mai puține celule care sunt tipuri de blocuri care constituie un organism complex. Indiferent dacă celula este un sistem holistic de viață - un organism separat sau este doar o parte din ea, este dotată cu un set de caracteristici și proprietăți comune tuturor celulelor.
Compoziția chimică a celulelor

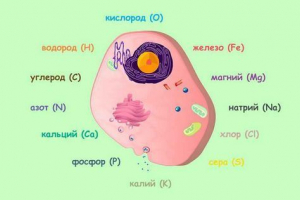
Aproximativ 60 de elemente ale periodice periodice Mendeleev, găsite în natură neînsuflețire, au fost găsite în celule. Aceasta este una dintre dovezile comunității de natură vie și inanimată. În organismele vii sunt cele mai frecvente hidrogen, oxigen, carbon și azot, care reprezintă aproximativ 98% din masa celulelor. Acest lucru se datorează particularităților proprietăților chimice ale hidrogenului, oxigenului, carbonului și azotului, ca urmare a cărora s-au dovedit a fi cele mai potrivite pentru formarea de molecule care îndeplinesc funcții biologice. Aceste patru elemente sunt capabile să formeze legături covalente foarte puternice prin împerecherea electronilor aparținând celor doi atomi. Atomii de carbon asociați covalent pot forma cadre de nenumărate multe molecule organice diferite. Deoarece atomii de carbon formează cu ușurință legături covalente cu oxigen, hidrogen, azot, precum și cu sulf, moleculele organice ajung la o complexitate excepțională și o varietate de structuri.
În plus față de cele patru elemente principale dintr-o celulă în cantități vizibile (10Y și 100Y Procentul de interes) sunt conținute fier, potasiu, sodiu, calciu, magneziu, clor, fosfor și sulf. Toate celelalte elemente (zinc, cupru, iod, fluor, cobalt, mangan si etc.) sunt într-o cușcă în cantități foarte mici și, prin urmare, se numesc oligoelemente.
Elementele chimice fac parte din compușii anorganici și organici. Compușii anorganici includ apă, săruri minerale, dioxid de carbon, acid și bază. Conexiunile organice sunt Proteine, acizi nucleici, carbohidrați, Gras (lipide) și Lipoids.
Unele proteine conțin sulf. O parte din acizii nucleici este fosfor. Hemoglobina molecula include fier, magneziu participă la construirea unei molecule clorofilă. Microelemente, în ciuda conținutului extrem de scăzut în organismele vii, joacă un rol important în procesele vieții. Iod Incluse în hormonul glandei tiroide - tiroxinei, cobalt - în compoziția vitaminei în12Hormonul insulei parte a pancreasului - insulina - contine zinc. În unele pește, locul de fier în moleculele de pigmenți care transportă oxigenul ocupă cupru.
Substanțe anorganice

Apă
N2O - cea mai comună conexiune în organismele vii. Conținutul său în diferite celule fluctuează în limite destul de largi: de la 10% în smalțul dinților până la 98% în corpul meduzei, dar este de aproximativ 80% din greutatea corporală. Un rol extrem de important al apei în asigurarea proceselor de viață se datorează proprietăților sale fizico-chimice. Polaritatea moleculelor și capacitatea de a forma legături de hidrogen face apă cu un solvent bun pentru o cantitate imensă de substanțe. Cele mai multe reacții chimice apar într-o celulă pot apărea numai în soluție apoasă. Apa participă la numeroase transformări chimice.
Numărul total de legături de hidrogen între moleculele de apă variază în funcție de tÎn. Cu TÎn Topirea gheții distruge aproximativ 15% din legăturile de hidrogen, la 30 ° C - jumătate. La trecerea la starea gazoasă, toate legăturile de hidrogen sunt distruse. Aceasta explică capacitatea de căldură specifică ridicată a apei. Cu o schimbare a unui mediu extern, apa absoarbe sau evidențiază căldura datorită unei rupe sau o nouă formare a legăturilor cu hidrogen. În acest mod de fluctuație t ° în interiorul celulelor sunt mai mici decât în mediul înconjurător. Căldura ridicată a evaporării stă la baza mecanismului efectiv de transfer de căldură în plante și animale.
Apa ca un solvent participă la fenomenele de osmoză care joacă un rol important în viața celulei organismului. Osmoza se numește pătrunderea moleculelor de solvent printr-o membrană semi-permeabilă într-o soluție de orice substanță. Semipermenii sunt numiți membrane care sări peste moleculele de solvent, dar lipsesc moleculele (sau ionii) substanței dizolvate. În consecință, osmoza este difuzia unilaterală a moleculelor de apă în direcția soluției.
Saruri minerale

Majoritatea celulelor B-în celulele anorganice sunt sub formă de săruri în stare disociată sau într-o stare solidă. Concentrația de cationi și anioni în celulă și în mediul înconjurător. Celula conține destul de mult la și o mulțime de na. În mediu extracelular, de exemplu, în plasma din sânge, în apă de mare, dimpotrivă, o mulțime de sodiu și puțin potasiu. Irigarea celulei depinde de raportul dintre concentrațiile de ioni na+, K+, Cca2+, Mg2+. În țesuturile animalelor multicelulare, K face parte dintr-o substanță multicelulară care asigură ambreiajul celulelor și locația comandată. Presiunea osmotică în celulă și proprietățile sale tampon depind de concentrația de săruri. Buffoff este capacitatea celulei de a menține o reacție slab familiară a conținutului său la un nivel constant. Bufferarea în interiorul celulei este furnizată în principal de ioni2RO4 și nra42-. În fluidele extracelulare și în sânge, rolul tamponului este jucat de2ASA DE3 și nso3-. Anioni se leagă ioni H și ioni de hidroxid (el-), astfel încât reacția din interiorul celulelor de fluide extracelulare nu este practic schimbată. Sărurile minerale insolubile (de exemplu, Phosfor CA) asigură rezistența vertebratelor osoase și a chiuvetelor de molusk.
Celulele organice ale celulelor
Proteine
Printre substanțele organice, celulele proteinelor sunt în primul rând în număr (10 - 12% din masa totală a celulei) și valoarea. Proteinele sunt polimeri cu greutate moleculară mare (cu o greutate moleculară de la 6000 la 1 milion. și mai sus) ale căror monomeri sunt aminoacizi. Organismele vii folosesc 20 de aminoacizi, deși există mult mai mult. Compoziția oricărui aminoacid include o grupare amino (-NH2), având proprietăți de bază și grupul Carboxyl (-son) având proprietăți acide. Doi aminoacizi sunt conectați într-o singură moleculă prin stabilirea comunicării HN-CO cu eliberarea moleculei de apă. Relația dintre grupul amino a unui aminoacid și carboxilul este o altă peptidă numită. Proteinele sunt polipeptide care conțin zeci și sute de aminoacizi. Moleculele diferitelor proteine diferă unul de celălalt cu greutate moleculară, număr, compoziție de aminoacizi și secvența locației lor în lanțul polipeptidic. Este clar că proteinele se disting printr-un imens varietate, numărul lor de toate tipurile de organisme vii este estimat de numărul de 10zece - Zece12.
Lanțul de unități de aminoacizi conectate prin legături de peptidă covalente într-o anumită secvență se numește structura primară de proteine. În celule, proteinele au vedere la fibre sau bile răsucite spirale (globule). Acest lucru se datorează faptului că, în proteina naturală, lanțul de polipeptidă este prevăzut strict într-un anumit mod, în funcție de structura chimică a aminoacizilor incluși în compoziția sa.

Inițial, lanțul polipeptidic se transformă într-o spirală. Există o atracție între atomii de viraje vecine și legături de hidrogen formate, în special între NH- și grupele situate pe rotiri adiacente. Lanțul de aminoacid, răsucite sub forma unei spirale formează o structură secundară de proteine. Ca urmare a unei poziții ulterioare a spirală, apare o configurație specifică pentru fiecare proteină, numită structura terțiară. Structura terțiară se datorează acțiunii forțelor ambreiajului între radicalii hidrofobi disponibili în unele aminoacizi și legături covalente între grupele SH Cistein aminoacid (S-S-Communication). Numărul de aminoacizi cu radicali hidrofobi și cisteină, precum și ordinea locației lor în lanțul de polipeptidă sunt specifice pentru fiecare proteină. În consecință, particularitățile structurii proteinei terțiare sunt determinate de structura sa primară. Activitatea biologică a proteinei prezintă numai sub forma unei structuri terțiare. Prin urmare, înlocuirea chiar de un aminoacid din lanțul polipeptidic poate duce la o schimbare a configurației proteinei și la o scădere sau pierdere a activității sale biologice.
În unele cazuri, moleculele de proteine sunt combinate între ele și își pot îndeplini funcția numai sub formă de complexe. Deci, hemoglobina este un complex de patru molecule și numai într-o astfel de formă se poate atașa și transporta. Astfel de agregate sunt o structură de proteine din țară. În ceea ce privește compoziția sa, proteinele sunt împărțite în două clase principale - simple și complexe. Proteinele simple constau doar din aminoacizi acizi nucleici (nucleotide), lipide (lipoproteine), UI (metaloprotede), P (fosfoproproide).
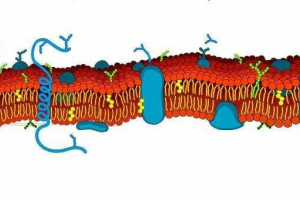
Funcțiile proteinelor din celulă sunt extrem de diverse. Una dintre cele mai importante funcții de construcție: proteinele sunt implicate în formarea tuturor membranelor celulare și a celulelor celulei, precum și a structurilor intracelulare. Rolul enzimatic (catalitic) al proteinelor este extrem de important. Enzimele accelerează reacțiile chimice care apar într-o celulă, în 10Ki și 100n Milioane de ori. Funcția motorului este asigurată de proteine contractuale speciale. Aceste proteine sunt implicate în toate tipurile de mișcări la care celulele și organismele sunt capabile de: pâlpâirea cilia și bătăile de arome de la cea mai simplă, abrevierea mușchilor la animale, mișcarea frunzelor în plante etc. Funcția de transport a proteinelor este aceea de a atașa elementele chimice (de exemplu, hemoglobina se alătură) sau substanțe biologice active (hormoni) și le transferă în țesuturi și corpuri corporale. Funcția de protecție este exprimată sub formă de dezvoltare a proteinelor speciale numite anticorpi, ca răspuns la penetrarea în corpul de proteine străine sau celule. Anticorpii se leagă și neutralizează substanțele străine. Proteinele joacă un rol important ca surse de energie. Cu divizarea completă 1G. Proteinele se remarcă la 17,6 kJ (~ 4,2 kcal).
Carbohidrați

Carbohidrați sau zaharide - substanțe organice cu formula generală (CH2O)N. În majoritatea carbohidraților, numărul atomilor de atomi sunt mai mari decât numărul de atomi, ca în moleculele de apă. Prin urmare, aceste substanțe au fost numite carbohidrați. Într-o cușcă vie, carbohidrații sunt în cantități care nu depășesc 1-2, uneori 5% (în ficat, în mușchi). Cel mai bogat în celulele de legume carbohidraților, unde conținutul lor ajunge în unele cazuri 90% din masa de materie uscată (semințe, tuberculi de cartofi etc.D.).
Carbohidrații sunt simpli și complexi. Carbohidrații simpli sunt numiți monozaharide. În funcție de numărul de atomi de carbohidrați din molecula de monozaharidă, ele sunt numite trioase, tetroze, pateosas sau hexoze. Din șase monozaharide de carbon - hexose - glucoză, fructoză și galactoză au cea mai importantă importanță. Glucoza este conținută în sânge (0,1-0,12%). Riboza și deoxisozoza pendes fac parte din acizi nucleici și ATP. Dacă două monozaharide sunt combinate într-o singură moleculă, o astfel de conexiune se numește dizaharidă. Zahărul alimentar obținut din zahăr sau sfeclă de zahăr constă dintr-o moleculă de glucoză și o moleculă de fructoză, zahăr din lapte - de la glucoză și galactoză.
Carbohidrații complexi formați din mai multe monozaharide sunt numite polizaharide. Monomer de astfel de polizaharide, cum ar fi amidonul, glicogenul, celuloza, este glucoza. Carbohidrații efectuează două funcții principale: construcții și energie. Celuloza formează pereții celulelor vegetale. Chitina polizaharidă sofisticată servește ca principală componentă structurală a scheletului exterior al artropodelor. Funcția de construcție a chitinei este efectuată de ciuperci. Carbohidrații joacă rolul sursei principale de energie în celulă. În procesul de oxidare 1 g. Carbohidrații lansați 17,6 kJ (~ 4.2 kcal). Amidonul în plante și glicogen la animale sunt depozitate în celule și servesc drept rezervă de energie.
Acizi nucleici

Valoarea acizilor nucleici din celulă este foarte mare. Caracteristicile structurii lor chimice oferă posibilitatea depozitării, transferului și transmiterii prin moștenire de către celulele copilului de informații privind structura moleculelor de proteine, care sunt sintetizate în fiecare țesut într-o anumită etapă a dezvoltării individuale. Deoarece majoritatea proprietăților și semnelor de celule se datorează proteinelor, este clar că stabilitatea acizilor nucleici este cea mai importantă condiție pentru durata de viață normală a celulelor și a organismelor întregi. Orice modificări ale structurii celulelor sau a activității proceselor fiziologice în ele, care afectează activitatea vitală. Studiul structurii acizilor nucleici este extrem de important pentru înțelegerea moștenirii caracteristicilor organismelor și a modelelor de funcționare, atât a celulelor individuale, cât și a sistemelor celulare - țesuturi și organe.
Există 2 tipuri de acizi nucleici - ADN și ARN. ADN - polimer constând din două spirale nucleotidice, prizonieri, astfel încât să se formeze spirale duble. Molomerii moleculelor ADN sunt nucleotide constând dintr-o bază de azot (adenină, timină, guanină sau citozină), carbohidrați (deoxiriboză) și acid fosforic. Bazele de azoty din molecula ADN sunt interconectate cu un număr diferit de n-link-uri și sunt situate în pereche: adenina (A) este întotdeauna împotriva timinei (t), guaninei (D) împotriva citozinei (c).
Nucleotidele sunt conectate unul cu celălalt nu întâmplător, ci selectiv. Abilitatea de a pune la dispoziție a adeninei cu chime și guanină cu citozină este numită complementară. Interacțiunea complementară a anumitor nucleotide se explică prin particularitățile aranjamentului spațial al atomilor în moleculele lor care le permit să închidă și să formeze n-obligațiuni. Într-o lanț de polinucleotidă, nucleotidele adiacente sunt interconectate prin zahăr (deoxiriboză) și reziduul acidului fosforic. ARN, precum și ADN-ul este un polimer al cărui monomeri sunt nucleotide. Bazele azotate ale a trei nucleotide sunt aceleași ca parte a ADN-ului (A, G, C) - cel de-al patrulea - Uracil (Y) este prezent în molecula de ARN în loc de timbru. Nucleotidele ARN sunt diferite de nucleotidele ADN și de structura carbohidratului inclus în compoziția lor (riboză în loc de dysoxiriboză).
În lanțul ARN al nucleotidelor sunt combinate prin formarea legăturilor covalente între nervura unei nucleotide și reziduul acidului fosforic al altui. Structura diferă două ARN cu lanț. Două lanțuri RNA sunt păzitori de informații genetice într-un număr de viruși, t.E. Acestea îndeplinesc funcțiile cromozomilor. Un lanț de transfer de ARN informații despre structura proteinelor de la cromozom la locul sintezei lor și participă la sinteza proteinelor.
Există mai multe tipuri de ARN cu lanț. Numele lor se datorează funcției sau locației din celulă. Majoritatea ARN-ului citoplasmatic (până la 80-90%) este un ARN ribozomal (RRNA) conținut în ribozomi. Moleculele RRNA sunt relativ mici și constau în medie de 10 nucleotide. Un alt tip de ARN (IRNN) care transportă informații despre secvența de aminoacizi din proteine care urmează să fie sintetizate la ribozomi. Dimensiunea acestor ARN depinde de lungimea secțiunii ADN pe care au fost sintetizate. ARN de transport Efectuați mai multe funcții. Ele livrează aminoacizii la locul sintezei proteinei, "recunoaște" (pe principiul complementarității) triplet și ARN corespunzător aminoacidului portabil efectuează orientarea exactă a aminoacidului pe ribozom.
Grăsimi și lipide

Grăsimile sunt compuși de greutăți moleculare grase și glicerină de alcool tricolar. Grăsimile nu se dizolvă în apă - sunt hidrofobi. Există întotdeauna alte substanțe complexe de grăsime hidrofobe în cușcă, numite Lipoids.Una dintre principalele funcții ale grăsimilor este energia. În timpul divizării 1 g. Grăsimi la S2 si n2Despre o cantitate mare de energie este scutită - 38,9 kJ (~ 9,3 kcal). Conținutul de grăsimi din celulele variază în intervalul de 5-15% din masa de materie uscată. În celulele țesuturilor pline de viață, cantitatea de grăsime crește la 90%. Funcția principală a grăsimilor din lumea animală (și parțial - legume) - stocare.
Cu oxidare completă de 1 g de grăsime (la dioxid de carbon și apă), se distinge aproximativ 9 kcal de energie. (1 KCAL = 1000 Calcalo (CAL, CAL) - o unitate incidentă a cantității de muncă și energie egală cu cantitatea de căldură necesară pentru încălzirea 1 ml de apă la 1 ° C cu o presiune atmosferică standard de 101,325 kPa-1 kcal = 4,19 kJ). Atunci când oxidarea (în organism), 1 g de proteine sau carbohidrați este alocată doar aproximativ 4 kcal / g. La o varietate de organisme de apă - de la diatomele unicelulare ale algelor la rechinii giganți - grăsimea este căutată de un "flotor", reducând densitatea medie a corpului. Densitatea grăsimii animale este de aproximativ 0,91-0,95 g / cm³. Densitatea osoasă vertebrate aproape de 1.7-1.8 g / cm³, iar densitatea medie a celor mai multe alte țesuturi este aproape de 1 g / cm³. Este clar că grăsimea are nevoie foarte mult de "echilibru" un schelet greu.
Grăsimile și lipidele efectuează funcția de construcție: fac parte din membranele celulare. Datorită scăderii termice, grăsimea este capabilă să protejeze funcția. La unele animale (sigilii, balene), este amânată în țesutul adipos subcutanat, formând un strat cu o grosime de până la 1 m. Formarea unor lipici precede sinteza unui număr de hormoni. Prin urmare, aceste substanțe sunt inerente în funcție de reglarea proceselor metabolice.